细胞种を直接変换させる低分子化合物を予测できる
机械学习アルゴリズムを开発
― 転写因子を模倣する、より低リスクな化合物の探索 ―
九州工业大学大学院情報工学研究院の濱野桃子助教?岩田通夫准教授、名古屋大学大学院情報学研究科の山西芳裕教授の研究グループは、国立研究開発法人産業技術総合研究所安全科学研究部門の竹下潤一主任研究員との共同研究により、iPS細胞を介さずに、すでに分化した細胞を別の種類の細胞へと直接変換するダイレクトリプログラミングを誘導する低分子化合物(薬剤など)の組み合わせを予測する机械学习アルゴリズムを开発しました。
ポイント
- すでに分化した細胞を別の種類の細胞へと直接変換するダイレクトリプログミングを誘導する低分子化合物(薬剤など)の組み合わせを予測する机械学习アルゴリズムを开発した。
- ダイレクトリプログミングを诱导する転写因子の働きを模倣する低分子化合物の候补を情报科学的に提案することで、细胞のがん化のリスクを回避することに贡献できる。
- 提案手法は、今后の再生医疗分野における细胞治疗のための细胞作製法の开発に繋がることが期待される。
本研究グループは、すでに分化した細胞を別の種類の細胞へと直接変換するダイレクトリプログラミングを誘導する低分子化合物(薬剤など)を予測する机械学习アルゴリズムを开発しました。ダイレクトリプログラミングの誘導には転写因子の遺伝子の導入が一般的ですが、細胞のがん化のリスクがあることから、低分子化合物で誘導する方法の開発が切望されていました。そこで本提案手法では、ダイレクトリプログラミングを誘導する転写因子の働きを模倣する低分子化合物を情報科学的に予測する机械学习アルゴリズムを开発しました。まず、細胞が転写因子の導入によってダイレクトリプログラミングを誘導される際の特徴を遺伝子の発現パターンから捉えました。次いで、細胞が変換する過程で変化する遺伝子発現パターンを模倣する低分子化合物の最適な組み合わせを探索しました。シミュレーティッドアニーリングの枠組みで開発した最適化アルゴリズムにより、ダイレクトリプログラミングを誘導する低分子化合物の組み合わせを予測することに成功しました。提案手法により、転写因子に置き換わる低分子化合物を簡便に予測することができるようになり、今後の再生医療分野における細胞作製法の開発を促進することが期待されます。
本研究成果は、2024年1月25日に叠颈辞颈苍蹿辞谤尘补迟颈肠蝉で公开されました。
■ 研究の背景と経緯
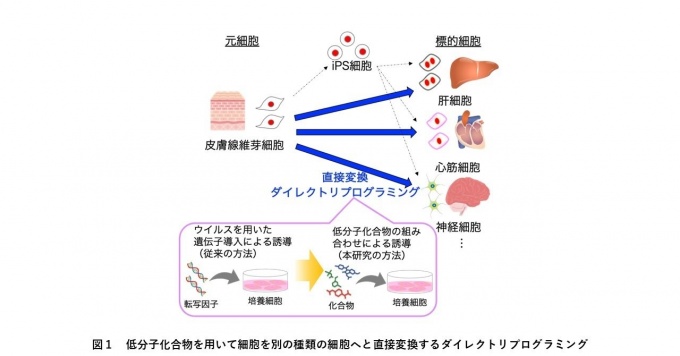
ダイレクトリプログラミングとは、iPS 細胞のような未分化の細胞を介さずに、すでに分化した細胞を別の種類の細胞に直接変換する技術です。短期間で低コストに細胞を作製できることから、転写因子※1の導入によるダイレクトリプログラミング誘導法の研究が注目されており、将来の再生医療を担う革新的な技術として期待されています。しかし、従来のダイレクトリプログラミングは、転写因子をコードする遺伝子を元細胞に導入するため、遺伝子導入に起因する細胞のがん化のリスクがありました。そこで近年では、発がんリスクを回避するため、低分子化合物※2(薬剤や化学物質など)を用いたダイレクトリプログラミングが注目されています(図1)。
ダイレクトリプログラミングを诱导する低分子化合物の最适な组み合わせを実験的に同定するのは膨大な実験コストがかかり、极めて困难です。また低分子化合物より転写因子の导入の方が细胞の変换効率が高いため、ダイレクトリプログラミングを诱导する方法は転写因子を中心に开発されており、低分子化合物による诱导法の开発は遅れています。そのため、近年蓄积されている生命科学ビッグデータを有効活用し、ダイレクトリプログラミング诱导転写因子と同じ働きをする低分子化合物を予测する技术が切望されています。しかしながら、ダイレクトリプログラミング诱导転写因子に置き换わる低分子化合物を予测する手法は未だに确立されていませんでした。
■ 研究の内容
九州工业大学大学院情報工学研究院の濱野桃子助教?岩田通夫准教授、名古屋大学大学院情報学研究科の山西芳裕教授の研究グループは、国立研究開発法人産業技術総合研究所安全科学研究部門の竹下潤一主任研究員との共同研究により、ダイレクトリプログラミングを誘導する低分子化合物を予測する机械学习アルゴリズムを开発しました。
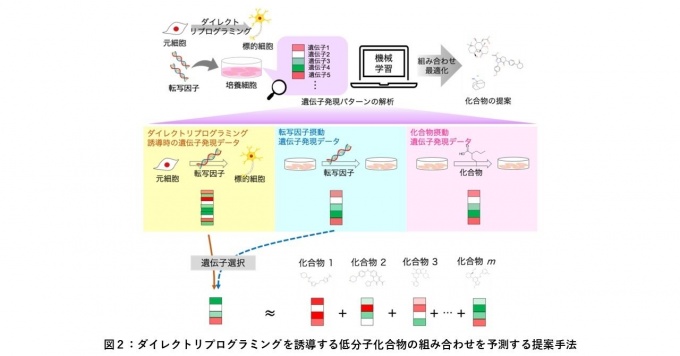
本研究の提案手法では、まず、ダイレクトリプログラミングを诱导することが知られている転写因子が细胞にもたらす遗伝子発现パターンの変化を调べました。次いで、その遗伝子発现パターンを模倣する低分子化合物の最适な组み合わせを探索するため、シミュレーティッドアニーリング※3の枠组みで最适化アルゴリズムを开発し、それを适用することでダイレクトリプログラミングを诱导する低分子化合物の组み合わせを予测しました(図2)。
ダイレクトリプログラミングを诱导することが実験的に証明されている転写因子の情报を基に、転写因子と同じ働きをする低分子化合物の组み合わせを予测した。転写因子によってダイレクトリプログラミングを诱导した际の遗伝子発现データからダイレクトリプログラミング诱导时の遗伝子発现パターンを特定する。次いで、ダイレクトリプログラミング诱导时に変化する遗伝子発现パターンを模倣する化合物の最适な组み合わせを発见するアルゴリズムを开発した。
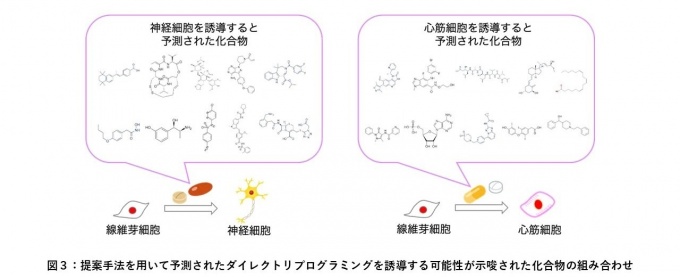
提案手法を用いて、線維芽細胞から神経細胞や心筋細胞への直接変換を誘導する低分子化合物を予測しました。その結果、10個の化合物の組み合わせが予測されました(図3)。予測された化合物群には、実験的にダイレクトリプログラミングを誘導することが証明されている既知の化合物であるTTNPB、Romidepsin、Etoposideが含まれており、統計学的有意に精度良く既知の化合物を再現できていることが分かりました。また、新規に予測された化合物には、神経活動に関与するシグナル経路であるNeuroactive ligand-receptor interactionを制御するMetaraminolやZafirlukastが含まれていました。心筋細胞を誘導すると予測された化合物として、心筋細胞へのダイレクトリプログラミングを誘導する制御パスウェイ※4として報告されているMAPK signalingやJAK-STAT signalingを制御するBnometinibやFigotinibが同定されました。これらの結果から、新規に予測された化合物群には各細胞の機能や分化を制御する化合物が含まれていることから、生物学的な妥当性が示唆されました。
线维芽细胞から神経细胞と心筋细胞への直接変换を诱导すると予测された化合物の组み合わせを示す。
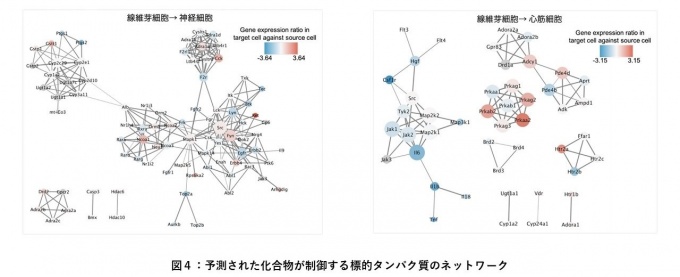
次いで、予測された化合物がダイレクトリプログラミングを誘導する分子メカニズムを理解するために、予測された化合物が作用するタンパク質を同定し、タンパク質間の共発現の関係性をネットワークとして確認しました(図4)。神経細胞を誘導すると予測された化合物群が作用するタンパク質ネットワークには、Mapk1, Src, Fynが高い中心性を持つタンパク質として同定されました。Mapk1はダイレクトリプログラミングを誘導する標的パスウェイであるMAPK signalingを構成するタンパク質です。また、SrcとFynは神経細胞のシグナル伝達系に関与することが報告されています。これらの結果から、神経細胞のダイレクトリプログラミングを誘導する化合物群は、ダイレクトリプログラミングに重要なパスウェイのタンパク質を網羅し、神経細胞への発達を誘導するシグナル伝達経路も制御することが分かりました。心筋細胞を誘導すると予測された化合物群が標的とするタンパク質ネットワークのうち中心性の高い標的タンパク質として炎症反応を誘導するサイトカインであるIL6が検出されました。心筋細胞へのダイレクトリプログラミングを促進する機構として、炎症反応を抑制することが報告されています。予測された化合物には抗炎症薬であるGamolenic acidが同定されており、それらを含む化合物を組み合わせることで、心筋細胞へのダイレクトリプログラミングを促進する可能性が示唆されました。
神経细胞を诱导すると予测された化合物群及び心筋细胞を诱导すると予测された化合物群が作用するタンパク质のネットワーク(左が神経细胞、右が心筋细胞)。ダイレクトリプログラミングが诱导される际の各タンパク质の遗伝子発现レベルを色で示している。
■ 今後の展開
本研究では、ダイレクトリプログラミングを誘導する化合物の組み合わせを予測する机械学习アルゴリズムを开発しました。提案手法は、ダイレクトリプログラミングを誘導する転写因子が制御する遺伝子発現パターンを模倣する化合物を見出す点が特長であり、また、その遺伝子発現パターンを基に最適な化合物の組み合わせをシミュレーティッドアニーリングによって予測する先駆的な情報技術です。
本提案手法は、ダイレクトリプログラミングを诱导する転写因子が明らかになれば、心筋细胞や神経细胞以外の细胞変换へ応用することができます。そのため、ダイレクトリプログラミングを诱导する方法が転写因子のみしか报告されていない细胞种に対しても适用することが可能です。このことから、本研究は再生医疗における细胞治疗法の开発への贡献に繋がることが期待されます。
本研究は、公益財団法人大川情報通信基金「安価で安全な再生医療を拓く情報技術基盤の構築」(研究代表者:濱野桃子)、JSPS科学研究費補助金?挑戦的研究(萌芽)JP18K19930「低分子化合物による転写因子制御と細胞直接変換のためのインシリコ予測法の開発」(研究代表者:山西芳裕)、JSPS科学研究費補助金?学術変革領域研究(B)JP20H05797「シナシ?ー効果を有する化合物群のAI による探索と設計」(研究代表者:山西芳裕)、挑戦的研究(開拓)JP21K18327「AIによるデータ駆動型ダイレクトリプログラミングの創生と腫瘍化リスクの回避」(研究代表者:山西芳裕)の支援を受け行われました。
■ 用語解説
※1 転写因子:DNA に結合して遺伝子の発現を調節するタンパク質。様々な転写因子を細胞に導入することで標的の遺伝子を発現調節することができる。
※2 低分子化合物:生物活性を有する化学物质や薬剤のこと。特定の生体分子(タンパク质)を标的として、その机能を阻害もしくは活性化する分子标的薬を含む。
※3 シミュレーティッドアニーリング:所望の条件を満たす最适解を探索するアルゴリズムの枠组みの一つ。焼きなまし法とも呼ばれる。
※4 生物学的パスウェイ:遗伝子やタンパク质の机能的な相互作用を経路として表したもの。代谢や遗伝子の制御関係、シグナル伝达系などの様々な种类のパスウェイが存在する。
■ 論文の詳細情報
| タイトル | “DIRECTEUR: Transcriptome-based prediction of small molecules that replace transcription factors for direct cell conversion” |
| 着者名 | Hamano, M., Nakamura, T., Ito, R., Shimada, Y., Iwata, M., Takeshita J., Eguchi, R. and Yamanishi, Y. |
| 雑 誌 | 「叠颈辞颈苍蹿辞谤尘补迟颈肠蝉」(オンライン版:1月25日) |
| D O I | 10.1093/bioinformatics/btae048 |
【研究に関するお问い合わせ先】
国立大学法人 九州工业大学大学院情報工学研究院
&别尘蝉辫;生命化学情报工学研究系 助教 滨野桃子
E-mail: momoko*bio.kyutech.ac.jp
TEL:0948-29-7831
東海国立大学機構 名古屋大学大学院情報学研究科
&别尘蝉辫;教授 山西芳裕
E-mail: yamanishi*i.nagoya-u.ac.jp
TEL:052-789-5638
【報道に関するお问い合わせ先】
国立大学法人 九州工业大学総務課広报係
E-mail: pr-kouhou*jimu.kyutech.ac.jp
TEL:093-884-3007
東海国立大学機構 名古屋大学広报課
E-mail: nu_research*t.mail.nagoya-u.ac.jp
TEL: 052-558-9735
&别尘蝉辫;(メールは*を蔼に変えてお送りください)